分子標的mTOR阻害薬が妊よう性温存の一助となる可能性
マウスを対象とした新たな研究の知見から、ある種のがん分子標的治療薬にはがん治療以外に別の用途がある可能性が示唆された。その別の用途とは妊よう性温存であり、がん治療を受けている一部の若年女性において適用できる。
このマウスを対象とした研究において、ニューヨーク州にあるニューヨーク大学のランゴン・メディカルセンターおよびパールマターがんセンターの研究チームは、mTOR(哺乳類ラパマイシン標的タンパク)阻害薬として知られる分子標的薬が不妊症の原因となる化学療法誘発性の卵巣損傷を防ぐことを明らかにした。
また、化学療法と併用してmTOR阻害薬を投与したマウスの産仔数は、化学療法のみを行ったマウスの産仔数よりもはるかに多かった、と研究チームはProceedings of the National Academy of Sciences誌3月7日号で報告した。
現在のところ、卵巣を損傷させる化学療法を受けている妊娠可能年齢にある女性の妊よう性温存に役立つ選択肢は複数ある。これらの選択肢にはゴセレリン(商品名:Zoladex[ゾラデックス])およびロイプロリド(商品名:Lupron[リュープロン])という2種類の薬剤がある。この2種類の薬剤は、化学療法中、卵巣保護のために卵巣機能を一時的に休止させる。別の選択肢には、卵母細胞(卵子)凍結保存法(卵子を採取後、将来の受精用に卵母細胞を凍結させる)、あるいは胚凍結保存法(卵子を採取後、子宮外で受精させ、胚として将来の着床用に凍結させる)がある。
しかし、両選択肢には限界があり、多くの少女と女性には適さない、と研究責任医師であるニューヨーク大学のランゴン不妊治療センターのKara Goldman医師は説明した。卵巣を化学療法から保護するのに役立つ薬剤があれば、前述のような妊よう性温存のための選択肢の代替法あるいは補完法として歓迎されるでしょう、とGoldman医師は述べた。
すでに3種類のmTOR阻害薬が臨床使用に関して承認を受けており、現在他のがんへの適応取得に向け、このタイプの複数の薬剤が研究されている。そしてmTOR阻害薬は、最終的に妊よう性温存治療薬として臨床研究に進むという「独特の位置にいる」とGoldman医師は続けた。
卵胞の休止状態を保つ
多くの化学療法薬は急速に分裂している細胞を標的とし、細胞DNAを障害する、と本研究の筆頭研究者であるRobert Schneider博士は説明した。シクロホスファミドは、乳がんに対する主な化学療法治療薬であり、生殖器にとって最も毒性の高い治療薬の1つである、とSchneider博士は述べた。
卵母細胞(未成熟な卵細胞)は、どのようなDNA損傷に対しても極めて鋭敏に反応する、と米国国立衛生研究所(NIH)の資金援助を受けるがん生殖医学協会のディレクターであるノースウェスタン大学フェインバーグ医科大学のTeresa Woodruff博士は説明した。たとえ小さいDNA損傷でも卵母細胞を細胞死させる可能性がある。
このDNA 損傷に対する「一触即発の反応」は卵母細胞が確実に「次世代に受け継ぐ(ゲノム的)正確性を保持する」ための防御機構である、とWoodruff博士は続けた。
また、化学療法は卵巣内の原始卵胞にも影響を及ぼす。原始卵胞は卵母細胞を保管し、活性化するまで通常は休止状態である。化学療法は特異的に原始卵胞のシグナル伝達経路を活性化する。この経路の活性化により原始卵胞が一次・二次卵胞への成熟を開始する。この過程により卵母細胞が最終的に放出されることになる。
この早期成熟により原始卵胞数が減少し、それにより卵巣予備能が低下するのだが、この現象は「卵胞のバーンアウト(burnout)」と知られている、とGoldman博士は説明した。
ゴセレリンは、卵胞の活性調整に関与するゴナドトロピンというホルモンの産生を鈍らせ、ゴナドトロピン感受性が高い卵胞を保護することで卵巣を一時的に休止状態にする。米国国立がん研究所(NCI)の資金援助を受けたPOEMS試験では、ゴセレリンを用いた治療により、乳がん治療を受けている閉経前女性の卵巣機能不全の発生率を低下させ、妊娠率を上昇させた。
したがって、研究チームは、ゴセレリンを用いた治療と同様の、化学療法中に原始卵胞が休止状態を保つ別の方法を探索している。
mTORは、原始卵胞が成熟卵胞への移行を開始する卵巣細胞におけるシグナル伝達経路の主要部分である。この移行中にmTORの活性が増強することが複数の研究で示されているため、研究チームはmTORの阻害によりこの移行が起きるのを防げる可能性が高いと推測した。
mTORを標的にすることは好ましい方針だ、とWoodruff 博士は述べた。たとえば、マウスの研究では、分子標的治療であるイマチニブ(商品名:Gleevec[グリベック])など、mTORと同じシグナル伝達経路を標的とする別の薬剤が原始卵胞の休止状態維持にも役立つことが示されている。
しかし、原始卵胞の早期活性化に関連する可能性がある要因およびシグナル伝達経路をすべて特定するために、さらなる研究が必要である、とWoodruff 博士は強調した。
原始卵胞が多いほど産仔数が多い
本研究においてランゴン・メディカルセンターチームは、一部の膵がん、腎がん、および乳がんの治療に対し米国食品医薬品局(FDA)承認を受けているエベロリムス(商品名:Afinitor[アフィニトール])および治験段階の第2世代mTOR阻害薬であるsapanisertib(INK128としても知られる)を検証した。
雌マウスにシクロホスファミドを投与すると、卵巣中の原始卵胞数が大幅に減少し、成熟卵胞数は上昇する。しかし、mTOR阻害薬と化学療法との併用によりマウスがより多くの原始卵胞を維持することができた。また、これらのマウスでは「臨床的に用いられる卵巣予備能に関する最も重要な指標の1つである」AMH(ホルモン)濃度がかなり高まったと研究チームは記した。
最終的に、研究チームが主要評価項目である妊よう性を調べると、化学療法へのmTOR阻害薬の追加は極めて有効であることを見いだした。化学療法のみを行ったマウスは不妊となるか受胎能が低下したが、一方、mTOR阻害薬+化学療法併用療法を行ったマウスのすべては妊娠率が正常であった。
さらに、化学療法のみを行ったマウスは、mTOR阻害薬+化学療法併用療法を行ったマウスと比べて、同腹の産仔数が平均して半数未満であった。
本研究で用いた薬剤用量はヒトで用いた場合とほぼ等量となるよう算出した、とGoldman博士は述べた。さらに、動物モデルの研究であり、治療関連の毒性評価には制限があったものの、併用療法を行ったマウスからは全く有害作用の徴候が認められなかった、と研究チームは報告した。
より低用量で検証し、試験を計画する
研究チームは、がん女性患者の妊よう性温存を目的としたmTOR阻害薬使用の初回臨床試験の立案など、次のステップを積極的に計画している、とSchneider博士は述べた。また、エベロリムス投与を受けている女性から血液検体を回収し、妊よう性に関連する重要な評価項目に及ぼす影響をすべて評価する研究も開始している。
また、より低用量の薬剤を用いても妊よう性温存について同じ結果を達成できるかについて確認することを目的とした動物モデルによる次段階の研究を開始しつつある。
「用量を抑えることが可能と考えています」とSchneider博士は述べた。発症頻度が高く消耗性のmTOR阻害薬の有害事象である口腔内の炎症性の痛み、いわゆる口内炎など、mTOR阻害薬の投与制限毒性を回避したいのです」とSchneider博士は述べた。
本研究で用いられた取り組みは期待できる、とWoodruff博士は述べた。しかし、mTOR阻害薬を妊よう性温存治療薬として臨床への移行可能とするには、まだ沢山すべきことがある、とWoodruff博士は注意を促した。その中には、mTOR阻害薬ががん治療の全体的な有効性にどの程度影響するか、また生存している卵母細胞において子孫に遺伝する可能性がある遺伝子変異の有無、についての評価が含まれる。
全体的にみて、がん治療を受けている患者の妊よう性の温存は、それ一つでどんな患者にも通用する解決法とはならないだろう、とWoodruff博士は続けた。新たな分子標的治療薬が利用可能となる中で、併用療法がますます多くなっているため、妊よう性の温存治療法の開発と検証は困難になっているだろう。
がん治療薬は「がん細胞だけでなく卵母細胞においてもそれぞれ異なる方法で作用する」、とWoodruff博士は述べた。「したがって、これらのがん治療が卵母細胞を活性化し損傷させる機序を理解するにつれ、治療ごとに個別化された卵巣保護療法を適用することができるようになるでしょう」。
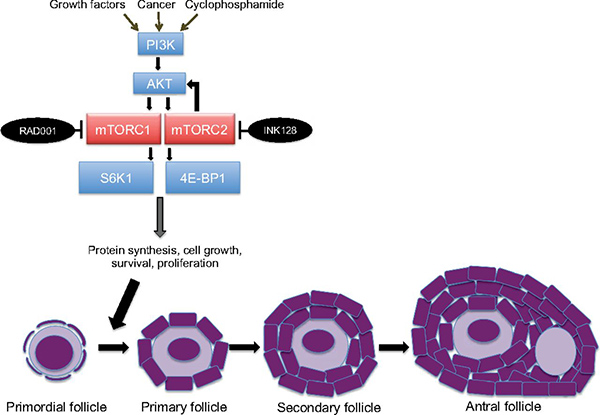
| 図キャプション:mTORタンパクは、休止状態の原始卵胞を刺激してより成熟した卵胞に移行させるという卵胞のシグナル伝達経路において重要な役割を果す。 |
原文掲載日
【免責事項】
当サイトの記事は情報提供を目的として掲載しています。
翻訳内容や治療を特定の人に推奨または保証するものではありません。
ボランティア翻訳ならびに自動翻訳による誤訳により発生した結果について一切責任はとれません。
ご自身の疾患に適用されるかどうかは必ず主治医にご相談ください。
がん治療に関連する記事
免疫療法薬が“効きにくいがん”を“効きやすいがん”に変える
2025年8月17日
患者自身の抗体が免疫療法薬の効果を高めるカギか
2025年8月12日
免疫細胞が「裏切り者」に―がんがNK細胞を再プログラムし免疫療法薬から回避
2025年8月6日
【ASCO2025】年次総会注目すべき追加研究・LBA ②
2025年7月18日




