2012/05/01号◆スポットライト「パワーの移入:癌治療のために患者自身の免疫細胞を利用する」
同号原文|
米国国立がん研究所(NCI)キャンサーブレティン2012年5月1日号(Volume 9 / Number 9)
~日経BP「癌Experts」にもPDF掲載中~
PDFはこちらからpicture_as_pdf
____________________
◇◆◇ スポットライト ◇◆◇
パワーの移入:癌治療のために患者自身の免疫細胞を利用する
| 2回シリーズの記事のうち初回は、養子細胞移入(ACT)と呼ばれる癌に対する免疫増強療法に関する記事であり、進行メラノーマを治療するために腫瘍浸潤リンパ球を用いるACTの一形態に焦点をしぼる。5月15日付のNCIキャンサーブレティンの第2回の記事では、遺伝子組換T細胞を用いて、さまざまな癌の治療のために研究されているACTの一形態について述べる予定である。また、ACTを小規模な臨床試験から日常診療で使用できるようにするうえでの課題についても考える。 |
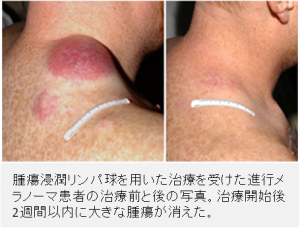 「この患者さんたちはおそらく治癒しています」とは、ほとんどの腫瘍専門医が進行癌患者について言えることではない。だが、NCIのDr. Steven Rosenberg氏は、NIH癌センターで主導した3件の小規模臨床試験で治療を受けた多数の進行メラノーマ患者について説明するのに、まさにこの言葉を使った。
「この患者さんたちはおそらく治癒しています」とは、ほとんどの腫瘍専門医が進行癌患者について言えることではない。だが、NCIのDr. Steven Rosenberg氏は、NIH癌センターで主導した3件の小規模臨床試験で治療を受けた多数の進行メラノーマ患者について説明するのに、まさにこの言葉を使った。
この試験では、患者(大半が体中に腫瘍が広がり[転移性疾患]、ほぼ他の治療選択肢を使い果たしていた)は、養子細胞移入(ACT)として知られる処置を受けた。
ACTでは、患者自身の免疫系細胞の一部を取り出し、数十億個を研究室で培養して、患者に戻す。これは、免疫系が独力でできる方法ではなく、腫瘍を攻撃できる免疫細胞の侵攻力を供給するという考えである。
「メラノーマにおける結果は印象的です」とRosenberg氏は述べた。同氏は、NCI癌研究センターの外科部門で同僚らとACTの先駆的な研究を10年以上行っている。
主にこの外科部門の成功に基づき、ACTをメラノーマに用いたり、他の癌にも拡大して研究プログラムを開始している研究者のグループは、米国内と外国で少数だがその数を増しつつある。
何らかの形態のACTで治療を受けた患者は、今のところ数百人にすぎないが、これまでに報告された有望な結果はさらに注目を集めており、いつの日かより多くの患者に利用できるだろうという希望がこの分野の研究者のあいだで高まっている。
TILが攻撃するとき
3件のNCIの試験で用いられたACTの手法では、患者の腫瘍検体から腫瘍浸潤リンパ球(TIL)というリンパ球を採取し、最大の抗腫瘍活性を持つ細胞はどれかを知るための検査を行い、その後、その特定の細胞を数週間にわたって研究室で培養する。
この1回限りの治療では、主にT細胞からなる新たに培養したリンパ球を、インターロイキン2(IL-2)と呼ばれるサイトカイン(免疫刺激因子)と共に、患者に戻す。
十分に高用量のIL-2は、それ自身で、メラノーマと進行腎癌患者の一部に対して、非常に効果的で治癒的ともいえる治療法であり得ると、外科部門上級研究者Dr. James Yang氏は説明した(IL-2は、両疾患を適応として米国食品医薬品局から承認を受けている)。しかし、投与が難しく、副作用が大きい場合があって、臨床現場での使用は非常に限られている。
拡大培養したTIL細胞の移入を受ける前に、患者は、一連の化学療法と現在の治療の形態の一つである放射線全身照射を受けることによりリンパ球枯渇状態となる。リンパ球枯渇療法により、「患者は障害なくリンパ球注入を受ける準備が整う」とYang氏は述べた。障害とは、注入される大量のT細胞の邪魔をする可能性のある他の免疫細胞などのことである。
これまでの結果は印象的である。3件の試験で治療を受けた93人の患者のうち、20人で腫瘍が完全に消滅(完全奏効)した。この20人のうち、19人で腫瘍なしの状態が5年を超えて持続した(これらの患者の大半の腫瘍は他の免疫療法に反応しなかった)。全体として、52人の患者で腫瘍が大幅に縮小した。
 一部の完全奏効の状態は8年を超えている。「私の見方では、それは、転移性メラノーマ患者の一部をおそらく治癒させることができるというよい証拠です。私は『治癒』という言葉を軽く使うことはありません」とRosenberg氏は述べた。
一部の完全奏効の状態は8年を超えている。「私の見方では、それは、転移性メラノーマ患者の一部をおそらく治癒させることができるというよい証拠です。私は『治癒』という言葉を軽く使うことはありません」とRosenberg氏は述べた。
Dr. Patrick Hwu氏は、NCIの外科部門で研修し、テキサス大学MDアンダーソンがんセンターで実施した進行メラノーマ患者の小規模臨床試験で同様の結果を得ている。MDアンダーソンで治療を受けた50人の患者のうち半数は部分的あるいは完全な腫瘍反応を示したと同氏は報告した。
TIL療法は「明らかに転移性メラノーマの最善の治療法の一つです」とHwu氏は述べた。NCI以外でTILと他の形態のACT療法を用いることは、研究上の重要なステップであると同氏は強調した。「私たちは、他の施設でもできることを証明しなければならなかったのです。」
その過程で、NCI、MDアンダーソンなどの確立した免疫療法プログラムに参加する研究者らは、施設自身のプログラムを構築する途中あるいは構築を希望している他の施設の研究者らと協議している。たとえば、Hwu氏らは、フロリダのモフィットがんセンターの免疫療法プログラムを確立するために同センターの研究者と協力した。
TIL療法は外国にも広まっている。Dr. Jacob Schachter氏は、イスラエルのシェバ医療センターでTIL療法を主導し、転移性メラノーマ患者で同様の結果を得ている。これまでに治療を受けた51人の患者のうち、6人が完全奏効、15人が部分奏効、多数の他の患者が病変安定を達成した。
「臨床的な反応があった人の70%が治療2年後にまだ存命しています」と同氏は述べた。
より良いものにする
この治療法は有望ではあるものの、克服すべき障害はある。他の癌の治療法と同様、TIL療法には副作用がある。IL-2、リンパ球枯渇に関連する毒性に加え、数十億ものT細胞注入は、患者にとって重篤で致死性にもなり得る問題を引き起こす可能性がある強烈な免疫反応の引き金となる場合がある。そして、一部の患者では、大量のT細胞を培養することはできない。
Schachter氏のグループは、「若い」TILに焦点をしぼって、この後者の問題に取り組もうとしている。それは、患者の腫瘍から採取したリンパ球の研究室での培養期間を短縮し、抗腫瘍活性を示すかどうかの検査による拡大培養のための選択を行わないという意味である。
こうした「若い」TILは、外科部門の研究者らも研究中で、「『選択されたTIL』よりも培養が比較的容易です」とSchachter氏は述べており、そのため研究者はより多くの患者に首尾よく治療を施すことが可能になっている。
外科部門の研究者らは、TILが癌細胞上の分子標的を見つけて狙いを定めたときにサイトカインのIL‐12を分泌するよう遺伝子操作したTILの試験を開始した。この治療を受けた最初の数人の患者で有望な結果が得られている。
MDアンダーソンのHwu氏らは、TIL療法を樹状細胞ワクチンやipilimumab(イピリムマブ、製品名Yervoy)などの他の免疫療法と組み合わせて用いている。また、癌細胞まで導く手助けをするケモカインとして知られる分子の受容体を発現するようにTILの遺伝子操作も行っている。
Hwu氏のプログラムの主要な焦点は、プロセス全体を標準化することだと同氏は述べた。「まだ、あらゆる患者のTIL細胞を首尾よく培養できていません。ですから、私たちは、最終生成物をより良くし、より多くの患者で細胞の培養を行える方法を常に探しています。」
TIL療法がさらに広く利用されるためには、たしかに課題があるとRosenberg氏は認めた。しかし、さらに研究を進め、支援を得て、経験を増せば、その課題は克服できると同氏は信じている。
「メラノーマのような命にかかわる病気になって、疾患の永続的な完全退縮を誘導できる治療法があるなら、皆その治療を欲するでしょう」と同氏は述べた。
—-Carmen Phillips
| 研究室からクリニックへ、そしてまた研究室へNCIの外科部門のTIL療法は、世界中の他の施設で研究中のACT療法の基礎となり、外科部門の研究者が主導する基礎研究やマウスモデルを用いた研究に基づいて精緻なものとなっている。たとえば、Dr. Nicholas Restifo氏が中心となって行われたマウスモデルを用いた研究では、放射線を照射することによるより強いリンパ球枯渇によって治療がさらに効果的になり、この知見からNCI主導のヒト対象の試験に用いられるTIL療法を同じように変えることになった。3件の試験のうち、最も高い線量の放射線照射を用いた試験では、完全奏効の達成率が最も高く25人のうち10人であり、そのうち9人の奏効状態は5年以上継続した。Dr. Rick Morgan氏は、IL-12を発現するように遺伝子操作したTILの基礎研究やマウスモデルを用いた研究を主導したが、それは重要な進展であった。なぜならIL-12はマウスで腫瘍を死滅させる力があるが、非常に毒性が強く、ヒトで全身に投与した場合、致死的になり得るからである。基礎研究と臨床現場とのやりとりというそのプロセスの性質は、外科部門の研究の土台である。「それは、NIH臨床センターとNIHの内部プログラムの非常にユニークな特徴だと思います」とYang氏は述べた。「ランチを共にし、クリニックで得た結果や、それを基礎研究にどう応用できるかを話し合うことができます。基礎研究で何が起こっているか、またそれをクリニックでの手法にどう影響させるべきかを話し合いました。これまで関わってきたどの研究よりも、速く生産的です」。 |
******
鈴木久美子 訳
大野 智(腫瘍免疫/早稲田大学・東京女子医科大学) 監修
******
原文掲載日
【免責事項】
当サイトの記事は情報提供を目的として掲載しています。
翻訳内容や治療を特定の人に推奨または保証するものではありません。
ボランティア翻訳ならびに自動翻訳による誤訳により発生した結果について一切責任はとれません。
ご自身の疾患に適用されるかどうかは必ず主治医にご相談ください。
皮膚がんに関連する記事
進行メラノーマに術前免疫療法(ニボルマブ+レラトリマブ)で4年後も無病状態を維持
2025年7月25日
● 87%の患者が治療4年後も生存し、...
【ASCO2025】年次総会注目すべき追加研究・LBA ①
2025年7月18日
学習済み機械学習モデルが資源の乏しい環境での非メラノーマ皮膚がん診断に有用
2025年5月10日
米FDAが転移/局所進行皮膚扁平上皮がんにcosibelimab-ipdlを承認
2025年2月1日





