2010/10/19号◆クローズアップ「共犯で癌細胞を死滅させる:合成致死性を利用した新標的の同定」
同号原文|
NCI Cancer Bulletin2010年10月19日号(Volume 7 / Number 20)
〜日経BP「癌Experts」にもPDF掲載中〜
____________________
◇◆◇ クローズアップ ◇◆◇
共犯で癌細胞を死滅させる:合成致死性を利用した新標的の同定
癌研究におけるこの1年の大きな話題の一つは、PARP(ポリADP-リボースポリメラーゼ)-1として知られる酵素を標的とした複数の薬剤の登場である。BRCA1あるいはBRCA2遺伝子のどちらかに変異を有する腫瘍など、特に治療が困難な乳癌の女性を対象とした初期段階の臨床試験で、このPARP1を阻害する薬剤が有望な結果を生んだ。(下記「関連記事」を参照)
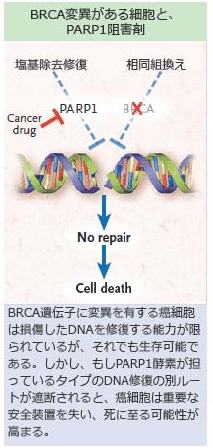
PARP1と同様に、2つのBRCA遺伝子は傷ついたDNAの修復を助けるタンパク質を産生する。このBRCA遺伝子に変異が生じると、正常細胞を癌細胞に変化させる可能性がある。しかしBRCA遺伝子変異に対してPARP1酵素を攻撃する治療を組み合わせることで、遺伝子的に不安定でありながらも癌細胞生存のための増殖を続けるのに必要な安全装置(フェイルセーフ)のメカニズムが排除される。つまり、これらの変異遺伝子とPARP1酵素は、「合成致死性」と呼ばれる関係となる。どちらかが単体で阻害あるいは損傷されても癌細胞に問題は生じないが、両方が共に阻害あるいは損傷された場合、癌細胞は消滅に向かうのである。
多くの腫瘍学研究グループは、高度なバイオインフォマティクスや、小分子あるいはRNA干渉(RNAi)スクリーニングといった比較的新しい手段を用いて、既存の治療標的、もしくは癌細胞のシグナル伝達ネットワークにおけるあまり知られていない構成要素のあいだの合成致死性の関係を同定しようとしている。これらの発見が、過剰な毒性、治療抵抗性および「新薬開発できない」標的といった腫瘍学における長年の問題の克服と新たな治療選択肢につながるかもしれないと、研究者らは考えている。
PARP1阻害剤の臨床試験結果が出る以前には、合成致死性は、ダナファーバー癌研究所のDr. William Hahn氏の言う「モデル生物で上手くいったのだからヒトでも上手くいくはずだという有望な論理上の概念」でしかなかった。「今やっと、患者のもとへ届けられ、臨床的有用性があると示されたことで人々は期待をしているのです」と同氏は続けた。
シグナル伝達ネットワークの中に当たりを見つける
合成致死性の概念は非常に魅力的であると、フォックスチェイスがんセンターで複数の合成致死関連プロジェクトに参加しているDr. Igor Astsaturov氏は述べた。正常細胞の大半は長い間にわたり休止状態であり、増殖関連シグナル伝達経路は間欠的にしか使われないと同氏は説明する。一方で、遺伝子的に不安定な癌細胞は「自ら有利になるように、持続的にシグナル伝達経路を使用します。だからこそ阻害に対して脆弱なのです」という。
フォックスチェイスでは、先月Science Signaling誌に発表されたAstsaturov氏らの知見の大部分をもとに、合成致死性を根拠とした治療法を検証する複数の臨床試験が計画されている。Astsaturov氏らの試験は、多くの癌に過剰発現するタンパク質である上皮細胞増殖因子受容体(EGFR)に重点を置いたものであった。EGFRは米国食品医薬品局(FDA)が認可した複数の抗癌剤の標的である。
本試験を行なうために、チームは徹底的に遺伝子およびタンパク質のデータベースを調べ、十分ではないが638種類のタンパク質の大規模な「ライブラリ」を構築した。これらのタンパク質は、EGFRがその主要素である広大な細胞内シグナル伝達ネットワークを構成している。研究者らはRNAiに基づいたスクリーニングを行い、いくつかの遺伝子産生物とEGFRとの間の合成致死関系を同定した。EGFRが薬剤により阻害され、また同時に一方の遺伝子発現が低分子干渉RNAによって排除されると、癌細胞死が増加したのである。
「この試験では多くの確実な手がかりが得られました」とAstsaturov氏は述べた。確実にEGFRとの合成致死性が認められる遺伝子産生物の大半は、EGFRの近くに集まっているか、EGFRと直接的、あるいは間接的な相互作用を有していた。非常に強い手ごたえがあったうちのいくつかは「探索的臨床研究に向けた併用療法のための理論上の標的を直接指し示しました」と同氏は続けた。その中にはオーロラキナーゼAおよびSTAT3転写因子などが含まれ、この2つは開発中薬剤の標的となっている。フォックスチェイス試験では、EGFR阻害剤をオーロラキナーゼA阻害剤と組合わせ、転移性肺癌および頭頚部癌の患者に使用する予定である。
現在の治療法の欠陥を回避する
合成致死性に基づいた癌治療の理論上の優位点の1つ(今ではこれを支持する複数の臨床エビデンスがある)が、毒性の低さである。というのも「損傷」がある細胞だけが合成致死性の関係を構築して(変異した遺伝子や治療で阻害された酵素など)この治療の影響を受けるためである。このような細胞は、ほとんど例外なく癌細胞であるはずである。PARP1阻害剤を検証した複数の試験でも、この薬による有害事象はほぼ現われなかった。
Hahn氏は次のように強調した。合成致死性に基づく治療法は、本来の生態あるいは標的の物理的組成のために「新薬の開発が不可能」となっている小分子や生物学的療法における標的の問題を克服する助けとなる可能性がある。最新の推計では、同定されている癌の分子標的のうち、このような問題があるものは75%にも及ぶという。
重要と考えられるが新薬開発につながらない標的の主な例としては、発癌遺伝子のKRASがある。これは膵臓、肺、また大腸など多くの癌で変異を起こしていることが多い。しかし、合成致死性がこの問題を回避する道を提供する可能性がある。
昨年、Hahn氏らはCell誌[とNature誌において、KRAS遺伝子変異を有する癌細胞株にRNAiスクリーニングを用いて、STK33およびTBK1の2つのキナーゼ酵素と、KRAS遺伝子との間の合成致死性の関係を調べた試験を発表した。試験ではキナーゼ(リン酸化酵素)が新薬開発につながる標的となることが判明している。Cell誌の同じ号で、ハーバード大学医学部のDr. Steven Elledge氏と同僚らは、PLK1と呼ばれる別のキナーゼを同定した。このキナーゼはKRAS変異と強力な合成致死関係を有する。
多くの合成致死研究が小分子またRNAiスクリーニングに頼っているが、PARP1とBRCA変異とのあいだの合成致死関係は以前のDNA修復の研究から推定され、臨床試験に移る前に、細胞株および動物モデルで検証された。(現在、研究者らはすでにPARP1と、標的となる他のDNA修復因子とのあいだの類似の関係を探索している)他の合成致死性の関係も、この方法で同定できる可能性があり、また同定できると考えられる一方で、本当に行うのは難しいだろう、とダナファーバー癌研究所のDr. William Kaeline氏は述べた。
細胞の分子ネットワークの基礎となっている生物学の理解は実質的に深まっているが「完全というところからはほど遠いのです」とKaelin氏は述べた。「イースト菌などといったモデル生物におけるスクリーニングから学んだのは、合成致死の相互作用を予測するのは難しいということです」。
疾患の個々の”ドライバー”を同定して標的とするのは実りある治療の道であるし今後もそうあり続けるだろうと同氏も考えている。しかし合成致死研究は、標的が宿る背景環境こそが重要なのだとはっきりと示している。「結局のところ、私たちが相手としているのは、単純な一本の経路というよりも、分子ネットワークなのです」。
ネットワークがどのように機能しているかについての理解を深めることで、さらに有用性が得られる可能性がある。つまり治療抵抗性の出現を防止することで、「交差耐性を起こさない、かつユニークな作用機序を持つ薬剤を組合せることで実現されるような有用性です」と同氏は述べた。
類似するものとして取り上げられるのがHIV治療の手段として使われる「カクテル」療法である。この考えは「腫瘍が抵抗性を獲得しないように押さえ込む」のだと、Golemis氏は説明した。「逐次治療を用いて、あるいはシグナル伝達ネットワークにおける複数のハブ遺伝子を攻撃する優れた併用療法を開発して、カクテル療法を行なうにせよ、目的を達成できるような手段を私たちは徐々に蓄積していきます」。
— Carmen Phillips
| 関連記事:治療が困難な乳癌にPARP阻害剤が有望DNA修復を仲介するPARPを標的とした開発中の薬剤が、転移性トリプルネガティブ乳癌を有する女性患者における生存期間を延長したと、米国の研究者らが先週ミラノで行われた欧州臨床腫瘍学会(ESMO)で発表した。121人の患者が参加した第2相臨床試験の最新の結果から、治療が困難なタイプの乳癌女性で、化学療法とPARP阻害剤Iniparib(イニパリブ)の併用療法を受けた患者では、化学療法のみを受けた患者と比較し、全生存期間が5カ月(12.3カ月対7.7カ月)改善したことが示された。試験でイニパリブとの併用療法を受けた患者は、化学療法のみを受けた患者と比べ、奏効率も高く、また無増悪生存期間も長かった。研究者らの報告によると、化学療法にイニパリブを追加してもそれに伴う有害事象は認められなかった。「これらのデータは有望で、現在のところ治療選択肢が限られている進行性トリプルネガティブ乳癌患者にとって、イニパリブが新たな治療選択肢となる可能性を示唆しています」と試験責任医師で、テキサス州のBaylor Charles A. Sammons Cancer Centerで乳癌研究プログラムを率いるDr. Joyce O’Shaughnessy氏はニュースリリース中で述べている。 |
******
岡田 章代 訳
原 文堅(乳腺科/四国がんセンター)監修
******
【免責事項】
当サイトの記事は情報提供を目的として掲載しています。
翻訳内容や治療を特定の人に推奨または保証するものではありません。
ボランティア翻訳ならびに自動翻訳による誤訳により発生した結果について一切責任はとれません。
ご自身の疾患に適用されるかどうかは必ず主治医にご相談ください。
がん研究に関連する記事
免疫細胞が「裏切り者」に―がんがNK細胞を再プログラムし免疫療法薬から回避
2025年8月6日
【米国癌学会(AACR)】MDアンダーソンから画期的発表12演題
2025年5月7日
がん細胞の弱点を見つける「金属探知機」を開発
2025年5月1日
ケンブリッジ大学の研究者らによって開発された...
休眠がん細胞にSTING作用薬で転移防止を目指す
2025年4月24日





